Kun kuuma lasi jäähtyy vapaasti, eli ilman, että sen jäähtymistä hidastetaan siihen tarkoitetuilla laitteilla, sen ulko- ja sisäosat jäähtyvät eri tahtiin. Niiden välille syntyy jännityksiä, jotka muuttavat lasin optiikkaa. Nämä jännitykset voidaan havaita polariskoopin avulla.
Seuraamalla lasin jäähtymisprosessia havaitaan, että jännityksiä syntyy sinne, missä lämpötilaerot ovat suurimmat. Osa jännityksistä purkautuu jäähtymisen aikana, kun lämpötilaerot tasautuvat.
Jännityksiä on eniten, kun lasi on 400–600-asteista. Tälle välille sijoittuu myös lasitransitiolämpötila, jossa esimerkiksi lasin lämpölaajeneminen muuttaa käyttäytymistään [1].
Polariskooppi
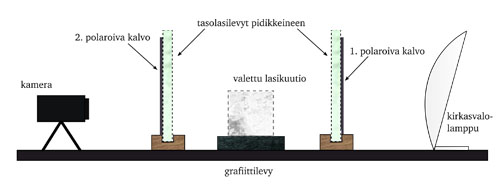
Polariskooppi tarkoittaa yksinkertaisimmillaan systeemiä, jossa kaksi lineaarisesti polaroivaa kalvoa asetetaan siten, että niiden läpi ei pääse valoa lainkaan. Kuvattava esine pannaan kalvojen väliin.
Jännitykset lasissa muuttavat valon polarisaatiota, jolloin niiden kohdalla kamerassa havaitaankin valoa.
Mitä kuvissa näkyy?

Esineet on kuvattu polariskoopin reunalla: vasemmalla puolella esineet näkyvät kuten paljain silmin; oikea puoli paljastaa lasissa kytevät jännitykset. Kuvien värit kertovat, minkälainen jännitys on kyseessä: punainen viittaa puristus- ja sininen vetojännitykseen [2].
Kuvista havaitaan, että veto- ja puristusjännitykset vuorottelevat ja saavat aikaan raidallisia kuvioita. Vapaasti jäähtyneen kuution keskustaan on kaasuuntunut ilmakupla ulkoreunojen nopean jäähtymisen takia.
Jännitykset aiheuttavat lasin hajoamisen kappaleiksi, mutta koska ne ovat paljain silmin näkymättömiä, vaikuttaa siltä, että räjähtäminen tapahtuu ilman syytä.
Teksti ja kuvat: Laura Aalto-Setälä.
Lähteet:
[1] Torquato, S., Nature 405 (2000)
[2] Falk, T. ym., Boken om glas, 2005


